Až o dva roky se může lišit prodleva mezi dnem, kdy je v Evropské unii zaregistrován nový inovativní lék, a dnem, kdy je tento lék vpuštěn do národního úhradového systému. To jsme napsali ve Zdravotnickém deníku před rokem. Letošní studie mapující rychlost přístupu pacientů v Evropě k inovativním léčivým přípravkům, kterou každoročně zpracovává analytická společnost IQVIA pro Evropskou federaci farmaceutických firem (EFPIA), ukazuje, že se toho od loňského roku příliš nezměnilo.
Analýza IQVIA letos zahrnula 39 evropských zemí (včetně 27 zemí EU) a 160 inovativních léčivých přípravků, které byly centrálně zaregistrovány v Evropské unii mezi lety 2017 a 2020. Z těchto 160 bylo 41 onkologických léků a 57 orphanů (léků na vzácná onemocnění). Hodnocen byl stav k 1. lednu 2022, tedy u kolika z těchto vybraných léků bylo na počátku letošního roku na národní úrovni dokončeno posouzení jeho ceny a úhrady.
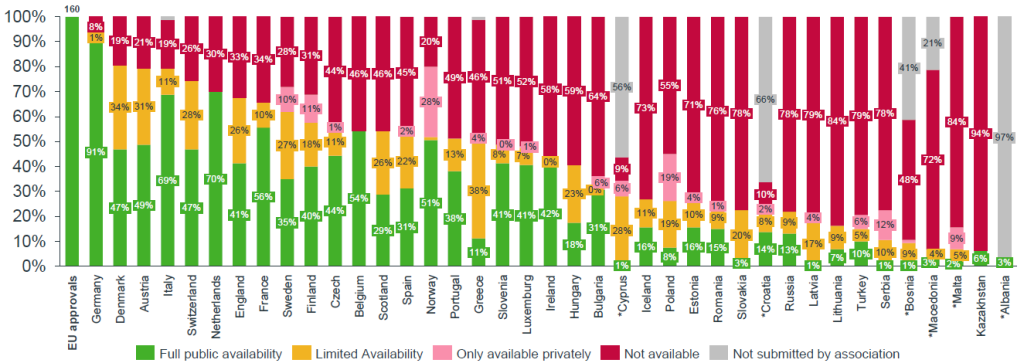
Z těchto 160 preparátů jich bylo na začátku letošního roku pacientům dostupných nejvíce v Německu (147) a ze zemí EU nejméně v Lotyšsku (26). Češi setrvávají na vcelku dobré pozici, tedy na místě jedenáctém (v rámci zemí EU místo deváté, vloni desáté) s 88 přípravky (tj. 55 procent z celkem registrovaných přípravků) s tím, že zhruba pětina z těchto léků je dostupná s nějakým omezením.
Podíváme-li se však na to, jak dlouho se čeká na stanovení úhrady již registrovaného léku, Česko se stále v žebříčku zemí EU se svými průměrnými 573 dny propadá dozadu, a to až za Slovensko (564 dní). Nejkratší dobu čeká pacient v Německu – 133 dní.
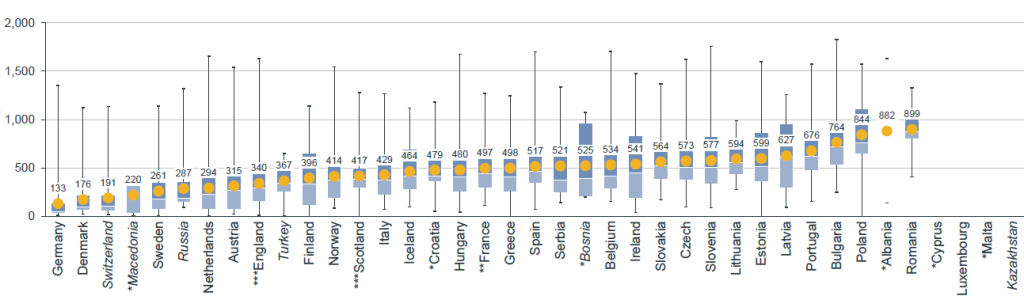
Ještě o něco hůře je na tom Česko při pohledu čistě na onkologické léky (657 dní) a orphany (660 dní). Český průměr vylepšují stejně jako vloni kombinované terapie, kdy se na schválení ceny a úhrady čeká „jen“ 437 dní.
Rozdíly v desítkách procent
EFPIA sdružuje inovativní farmaceutický průmysl, svoji studii tedy zaměřila na inovativní a často dosti nákladné léky. Ty obvykle v rámci EU schvaluje Evropská léková agentura (EMA) tzv. centralizovaným způsobem a registrace udělená agenturou platí ve všech státech EU najednou.
To však, jak ukazují zmíněná čísla, automaticky neznamená, že jsou pacientům hned k dispozici. V jednotlivých státech, včetně ČR, ještě probíhá vlastní, a mnohdy komplikované a časově náročné, cenové a úhradové posouzení. Až po jeho skončení je lék vpuštěn do systému a, minimálně částečně, pacientům hrazen.
V průměru bylo v Evropě ze zmíněných 160 přípravků vloni pacientům k dispozici necelá polovina (46 procent, vloni 49 procent) a trvalo to 511 (vloni 504) dní, než se zaregistrovaný lék dostal ke stanovení úhrady. Rozdíly mezi jednotlivými zeměmi jsou závratné, a to především ve srovnání zemí ze severní a západní částí Evropy a těch z jihu a východu.
Mohlo by vás zaujímať
Tak například z oněch 160 léků jich bylo k 1. lednu 2022 v Německu dostupných 147, ve Španělsku 85, ale v Rumunsku jen 38 a v Srbsku dokonce pouze 17. Období mezi schválením na trhu a stanovením úhrady se pohybuje od čtyř měsíců až po dva a půl roku, přičemž pacienti v jižní a východní Evropě čekají v průměru 600 až 850 dní.
Nerovnosti však existují i v rámci jednotlivých zemí. Zatímco v Německu mají pacienti plně k dispozici 91 procent hodnocených léků, v Polsku je to již jen osm procent, částečně je dostupných 19 procent a ke stejnému počtu léků se lidé dostanou pouze soukromě.
Současné platební modely „nestíhají“
Právě otázka příčin nedostupnosti léků v různých zemích je nyní velmi horkým tématem, a to především v souvislosti s očekávanou rozsáhlou novelizací unijní lékové legislativy, kterou eurokomisařka pro zdraví Stella Kyriakidesová předloží na konci tohoto roku. V rámci přípravných prací vydala k tomu vloni Evropská komise rozsáhlou studii, kde mezi příčinami výpadků identifikovala kromě problémů v rámci výrobního řetězce i nastavení národních úhradových mechanismů.
Otevřeně se také hovoří o tom, že současné platební modely si již neví rady s novými typy terapií, jako je genová a buněčná léčba. Ty často představují jednorázové zákroky s vysokými vstupními náklady, které nicméně nahrazují celoživotní nákladnější péči. Stanovení cen a úhrad je sice výsostnou záležitostí jednotlivých vlád, do níž nemá unijní exekutiva co zasahovat, ale časy se mění. Již ve své evropské lékové strategii z listopadu 2020 hovoří Kyriakidesová o tom, že je zapotřebí prohloubit spolupráci mezi státy a vyměňovat si zkušenosti a informace právě v těchto tak komplikovaných případech, které jsou nové nejen pro Českou republiku.
Helena Sedláčková

