Zatímco před několika desítkami let znamenalo nezřídka onkologické onemocnění ortel smrti, dnes dokáží lékaři i díky inovativním lékům zajistit mnoha pacientům vyléčení nebo výrazné prodloužení života. Řada těchto přípravků nejen na onkologické choroby však není hrazena v rámci standardního procesu, ale přes paragraf 16. Příčinou je mimo jiné to, že v Česku trvá stanovení maximální ceny a úhrady skoro nejdéle v Evropě. O nápravu tohoto stavu se nyní snaží jak Státní ústav pro kontrolu léčiv (SÚKL), tak v rámci systémovějších řešení také ministerstvo zdravotnictví. Otázkou však je, zda je náš systém z dlouhodobější perspektivy na rychlý vstup nákladných inovací vůbec připraven z hlediska finanční udržitelnosti. Problematikou se zabývali odborníci u kulatého stolu Zdravotnického deníku s názvem Dostupnost inovativních léků pro české pacienty. Kde jsme a kam směřujeme?, který se konal minulý týden v Praze.
„To, co dnes průmysl přináší, je to, co se mu léta vytýkalo, že nemá: nové léčivé přípravky. Podle kritiky dřív většina inovací byly pouhé úpravy stávajícího, kdy jsme nebyli schopni přinést na trh něco opravdu inovativního a zásadně jiného. To se v posledních cirka pěti, šesti letech děje. To, že jsou tu nové technologie, které jsou významně náročnější na výrobu, diagnostiku a další oblasti, se ale projevuje výrazným tlakem na rozpočet. Každý stát se proto musí rozhodnout, kam půjde a zda všechno, co nové technologie nabídnou, svým pacientům dopřeje,“ uvádí výkonný ředitel Asociace inovativního farmaceutického průmyslu (AIFP) Jakub Dvořáček.
Podle AIFP u nás loni získalo úhradu 73 originálních přípravků, z toho 22 nemělo dopad do zdravotnického rozpočtu (dva produkty byly navíc zamítnuty a jeden vyhodnocen jako nemocniční, získal tedy jen maximální cenu). Ze 48 léků s dopadem do rozpočtu jich téměř 60 procent spadalo do oblasti onkologie či hematoonkologie; 19 procent přípravků získalo dočasnou úhradu v režimu vysoce inovativních léčivých přípravků (VILP) a 17 procent dostalo trvalou úhradu po režimu VILP. Dohromady přitom budou mít léky s nově stanovenou úhradou v prvním roce dopad do rozpočtu ve výši 2,3 miliardy, předpokládají se ovšem slevy ve výši 10 až 40 procent.
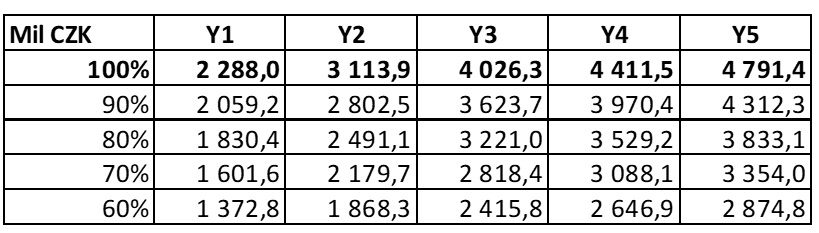
Problém však podle Dvořáčka představuje doba, po kterou našemu státu, potažmo lékovému ústavu, trvá, než novému léku schválí úhradu. V tomto parametru jsme totiž na chvostu Evropy. „Jsme na druhém nejhorším místě v celé Evropě. Situace je tedy kritická,“ konstatuje i místopředseda sněmovního zdravotnického výboru a gastroenterolog profesor Julius Špičák (za Ano).
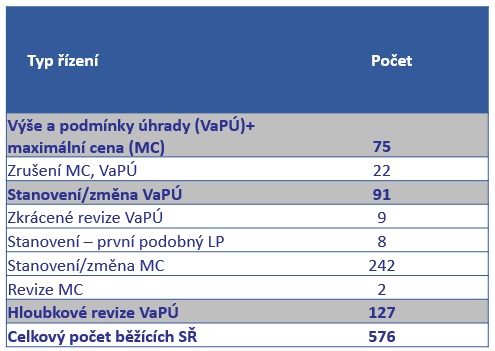
Lékový ústav přitom v tuto chvíli vede více než pět set správních řízení. „V uplynulém roce jsme se snažili nastavit systémy při posuzování co nejefektivněji a podívat se na jednotlivé kroky tak, abychom je zrychlili, zjednodušili a přiblížili se k zákonným lhůtám, které bychom měli plnit,“ uvádí Milan Vocelka ze Sekce cenové a úhradové regulace SÚKL.
V současnosti se tak daří zrychlovat vydání první hodnotící zprávy v řízeních zahájených v roce 2018 a letos by se měly lhůty dále zkracovat. „Bohužel to nejde tak rychle, jak bychom si přáli. Všechny procesy se musely revidovat, zaktualizovat a postupně se na ně zaměstnanci snaží přenastavovat,“ přiznává Vocelka.
Mohlo by vás zaujímať
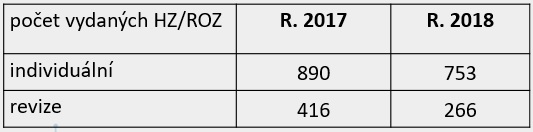
U lhůty od zahájení do vydání rozhodnutí je navíc zkrácení trvání zatím ještě menší, což je dáno i tím, že zde rychlost závisí na všech účastnících, nejen na SÚKL. Aby toho nebylo málo, podání mají nezřídka přes sto stran a loni navíc narostlo oproti počtu správních řízení množství hodnotících zpráv. Zatímco individuálních správních řízení proběhlo 120, hodnotících zpráv bylo vydáno skoro 200 (o rok dříve šlo o 79 správních řízení a 115 hodnotících zpráv). Na ústavu je přitom vyřizuje kolem 13 lidí.
Kde je příčina protahování? „Je to z různých důvodů, nejčastěji předpokládáme, že jde o risksharingové dohody mezi držiteli a zdravotními pojišťovnami. Zároveň se zdá, že důvodem mohou být i častější změny obsahu podání, kterých za uplynulé dva, tři roky přibylo dvojnásobně. Každou změnu v podání, kterou obdržíme, musíme vyhodnotit. Obvykle to není pouze o tom, že se navrhuje nižší úhrada, ale bývá to spojeno s podáním nové indikace a nových důkazů například pro změnu indikačních omezení. Pak se správní řízení velmi prodlužuje,“ vysvětluje Milan Vocelka.
Zlepšení situace ve zrychlování řízení každopádně potvrzuje i průmysl. „Změna k lepšímu tam je. Bohužel roky 2016 a 2017 vytvořily obrovský propad ve srovnání s dalšími evropskými státy, jak hluboko jsme se v řadě vstupování inovací dostali. Dnes se pohybujeme na průměru kolem 600 dní od podání žádosti po schválení, i když v roce 2018 je zlepšení performance výrazné,“ konstatuje Jakub Dvořáček s tím, že polovina originálních léků, které loni získaly úhradu, měla podání v letech 2017 či 2018. Průměrná doba do vydání první hodnotící zprávy přitom činila 361 dní (medián 205 dní, maximum 923 dní) a do přiznání úhrady 594 dní (medián 532 dní, maximum 1443 dní). Ve 46 procentech případů bylo správní řízení přerušeno, a to zejména z důvodu dohody s plátci, v 67 procentech byla uzavřena dohoda s plátci v podobě slevy nebo jiného mechanismu sdílení rizik uzavřena.
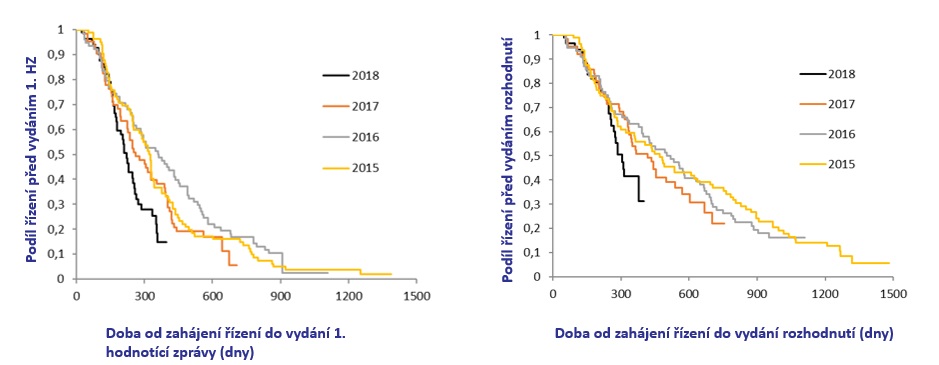
„Část času se přelila ze SÚKL k pojišťovnám – naprostá většina přerušení byla proto, abychom mohli vést negociaci se zdravotními pojišťovnami, což s sebou nese poměrně velkou náročnost na čas, byť i tam je vidět chuť hledat nová řešení v kontextu risksharingových schémat nebo outcome-based dohod,“ potvrzuje vysvětlení lékového ústavu Jakub Dvořáček.
Lékový ústav už řeší i posuzování moderních terapií
SÚKL přitom plánuje dále na zrychlování pracovat. Chce proto limitovat hloubkové revize pouze na případy, kde trvá zájem praktiků na rozvolnění preskripčního omezení. S tím souhlasí i ministerstvo zdravotnictví. „Nechceme, aby byl SÚKL zatěžován dalšími revizními řízeními a každých pět let zbytečně zahajoval stovky nových hloubkových revizí. Pojďme upravit procesní pravidla v zákoně 48 a nechme, aby revize byly dělány jen tam, kde to dává smysl – kde přichází biosimilars a generika, kde je patentový vliv nebo eroze cen v zahraničí. Dejme ale prostor SÚKL na to, aby se prioritně věnoval inovacím,“ poukazuje náměstek ministra zdravotnictví Filip Vrubel.
Vedle toho SÚKL připravuje jednotný formulář pro podání žádosti, který je momentálně ve fázi připomínkování české a anglické verze. Ty by měly být znovu v průběhu dubna rozeslány stakeholderům, na což bude navazovat seminář a vydání finální verze. Od změny si přitom lékový ústav slibuje snížení počtu výzev k součinnosti a právě urychlení správních řízení.

Další věcí, na které SÚKL pracuje, je zjednodušení hodnotící zprávy. Proto připravil dotazník pro všechny stakeholdery, kteří tak dostali možnost vyjádřit se k tomu, jaké informace jsou pro ně zásadní a v jaké podobě je preferují. Ústav dostal 38 dotazníků, které nyní zpracovává a snaží se je zohlednit v připravovaném návrhu. První verze by měla být rozeslána zřejmě během tohoto měsíce.
„Největším tématem pravděpodobně bude vytvoření metodiky pro posuzování úhrady přípravků pro moderní terapie. V poslední době přitom dostáváme dotazy, jak to vypadá s moderními terapiemi, co se týče procesu stanovení úhrady. SÚKL stanovuje úhradu opatřením obecné povahy, a to pouze u přípravků používaných v ambulantní péči. Spis opatření obecné povahy na rozdíl od správního řízení není veřejně dostupný, co se týče dálkového přístupu, ale dotčené subjekty mají možnost do něj nahlédnout fyzicky. O zahájení opatření obecné povahy informujeme na webových stránkách. Pro stanovení úhrady je nutno předložit kromě dokumentace i cenu registrovaného přípravku tak, aby mohla být vykalkulována úhrada,“ načrtává Vocelka.

Dokumentaci obdrženou od držitele registrace přitom úřad posuzuje ve spolupráci se zdravotními pojišťovnami a odbornými společnostmi tak, aby opatření obecné povahy zahrnovalo konsenzus na nákladech a indikačních omezeních. Na dokumentaci se vztahují standardní požadavky (tj. účinnost, bezpečnost, porovnání nákladů a přínosů plus dopad na rozpočet zdravotního pojištění), před podáním podnětu na SÚKL je ale možné požádat ústav o konzultaci. „Z prvních zkušeností zahraničních agentur se zdá, že není zásadní problém, co se týče kvality evidence nebo dosažení nákladové efektivity. V tomto ohledu tedy neočekáváme zásadní problém u kvality, chápu ale, že obavy o dopad na rozpočet jsou oprávněné,“ dodává Milan Vocelka (problematice nákladnosti přicházejících moderních terapií, jako je genová terapie, jsme se věnovali jako první v rámci jednoho z minulých kulatých stolů ZD, více zde či zde).
Novela ošetřující vstup inovací půjde do připomínek v nadcházejících týdnech
Náročnost správních řízení potvrzují také zdravotní pojišťovny. Léková komise Svazu zdravotních pojišťoven ročně jednotlivě projedná přes tisíc dokumentů k těmto řízením. Některé zprávy přitom mají i přes sto stránek a je jich v řízení několik (jedno z loni uzavřených správních řízení mělo dokonce sedm hodnotících zpráv). Na druhou stranu je pravda, že objem správních řízení lehce klesl, a to zejména u revizí, kterých bylo v roce 2017 416 a loni 266. „Možná číslo poukazuje, že potenciál revizí z hlediska úspor, které je pak možné věnovat na nové molekuly nebo rozšíření indikací, se nám tím zmenšuje,“ říká k tomu předsedkyně lékové komise SZP Kateřina Podrazilová.
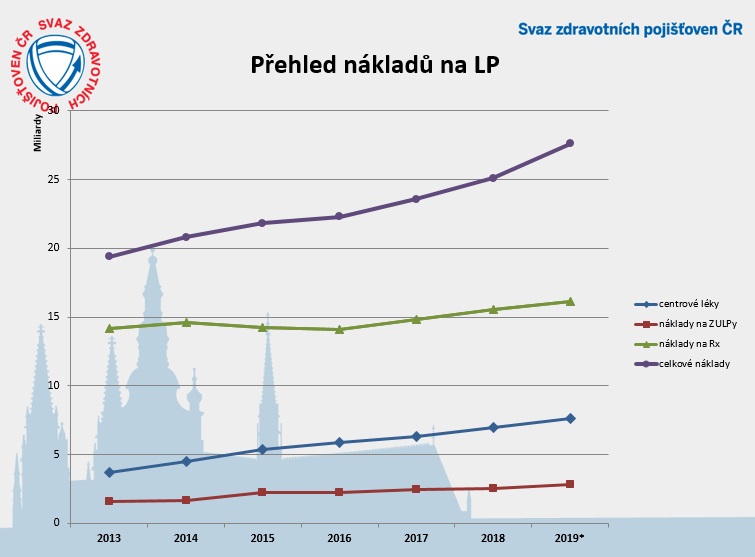
V současnosti tak stoupají náklady na všechny tři skupiny léčiv – ambulantní zvlášť účtované léčivé přípravky – ZULP (které spolknou nejméně peněz), centrové léky a už i receptové léky, což je zřejmě částečně dáno právě vyčerpáním potenciálu revizí. Podle Podrazilové by přitom právě tato kategorie mohla letos ještě výrazněji vzrůst spolu s tím, jak se rozvolňuje preskripce pro praktické lékaře.
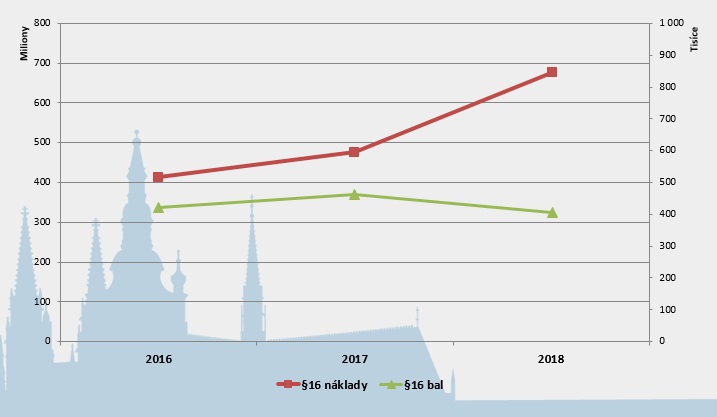
Zajímavý je trend sledovaný u nákladů na přípravky hrazené přes paragraf 16, které nemají stanovenou cenu a úhradu (jde o zhruba polovinu případů schvalovaných přes paragraf 16). Zatímco mezi roky 2016 a 2017 Svazu zdravotních pojišťoven mírně rostl počet balení i náklady, v roce 2018 došlo k výrazné změně – počet balení lehce klesl, ale náklady velmi vzrostly. „Přepočteno na balení platíme za nákladnější terapie,“ konstatuje Podrazilová.
I to je důvod, proč je třeba problém řešit systémově. Jak už jsme opakovaně informovali (například zde), takové změny chystá ministerstvo. Původně přitom předpokládalo, že novela ošetřující vstup inovativních přípravků a léků na vzácná onemocnění bude touto dobou v připomínkovém řízení, nakonec ale prioritně řešilo úpravu zaměřenou na výpadky léčiv, která jde nyní do meziresortu.
„V nejbližších týdnech bychom chtěli pustit do vnitřního připomínkového řízení návrh novely zákona 48, která reflektuje to, co bylo odsouhlaseno na pracovní skupině na přelomu tohoto a loňského roku, tedy základní pilíře pro vstup inovací do systému veřejného zdravotního pojištění. Očekávám, že celá řada účastníků snese v průběhu připomínkového řízení celou řadu požadavků na úpravy procesního i věcného charakteru. Dopředu říkám, že budeme otevření vyhovět, protože můžeme dát do novely věci, které nám tak vzhledem k délce legislativního procesu pomůžou dříve než na konci tohoto nebo až v průběhu dalšího volebního období,“ přibližuje náměstek Vrubel.

Už nyní je pak v připomínkovém řízení novela zákona 48 reagující na nález Ústavního soudu, která se týká posuzování zdravotních pojišťoven o nároku pojištěnce. „Řekli jsme si, že tuto část pustíme separátně, protože jsou tam trochu jiní stakeholdeři a diskuze tam právně a procesně bude vedena trochu jinak. Jakmile ale projde připomínkovým řízením i druhá část týkající se vstupu inovací, chceme novely spojit dohromady,“ dodává Vrubel.
Centrová péče v příštím roce vzroste zhruba o 2,5 miliardy
Jak ovšem ve věci vstupu inovací připomíná Julius Špičák, je také důležité říci, jaké léky tu chceme a jaké ne – ne všechny totiž mají pro pacienta stejný přínos. „Hraje tu důležitou roli stanovení účinnosti a sledování zahraničních guidelinů. Musím říci, že lékaři mají snahu nadsazovat očekávání. Oblast léků je velmi různorodá a ti, kdo je podávají, by měli být zavázáni, aby léčbu monitorovali, takže se po třech letech budeme moci vrátit a posoudit ji,“ domnívá se profesor Špičák.
Náměstek VZP David Šmehlík pak akcentuje také otázku nákladů a finanční udržitelnosti. „Očekáváme, že s procesními pravidly se budeme bavit i o nastavení rozumných úhradových pravidel, abychom zajistili udržitelnost systému. Vidíme, že náklady na léčivé přípravky obecně rostou velmi rychlým tempem. Pravidelně se kalkuluje horizont scanning, jak se budou vyvíjet náklady na centrovou léčbu. Začalo dohodovací řízení a predikce už proběhly analytickou komisí. Předpoklad, který je velmi konzervativní, je 2,5 miliardy korun. Víme také, že to, že pacienti z léčby profitují a setrvávají na ní delší dobu, vede ke kumulaci nákladů. Kombinace toho, že máme stále více inovativních léčivých přípravků ve stále větším počtu indikací a zrychlující se proces SÚKL, má silný dopad na náklady veřejného zdravotního pojištění. Doufáme ale, že zvýšené náklady u inovativních léků budou kompenzovány snížením nákladů u léčivých přípravků, které už byly generifikovány nebo máme biosimilars, aby byl systém udržitelný,“ uvádí David Šmehlík.

Na to poukazuje také Filip Vrubel. „Představme si, že by takový nárůst přišel za situace, v jaké byla ekonomika kolem roku 2012 a 2013. To bychom si dovolit nemohli. Bavíme se tady o nárokové péči, ne o paragrafu 16. Ve chvíli, kdy lék do systému pustíme, ho už ho pravděpodobně nikdy nebudeme schopni vyhodit,“ konstatuje náměstek Vrubel. Situaci navíc komplikuje výše nastíněný stav, kdy se rozevírají nůžky mezi incidencí a prevalencí – úspěšně léčení pacienti tak vyvíjejí další choroby, které vyžadují další náklady.
„Musíme tedy vnímat, že jestliže budeme zrychlovat vstup nových inovací, a to nejen u léčiv, ale i u přístrojové techniky a tak dále, musíme diskutovat systém financování zdravotního pojištění jako celek. A tady nejsme jako ministerstvo zdravotnictví jediným hráčem – pokud se bavíme o příjmech systému, je mnohem silnějším hráčem ministerstvo financí. Asi všichni zaznamenali diskuzi o změnách systému tvorby příjmů veřejného zdravotního pojištění, která znervóznila i ministerstvo zdravotnictví. To je věc, o které bychom měli diskutovat – neřešit jen partikulárně oblast vstupu inovací, ale systém financování obecně,“ říká náměstek Vrubel s tím, že se současnými výhledy se ve střednědobém či dlouhodobém horizontu ocitneme v situaci, kdy příjmy nebudou odpovídat poptávce. „Chceme rychlejší vstup inovací do systému, ale zároveň musíme diskutovat o tom, jak do systému dostat dodatečné finanční prostředky,“ uzavírá Vrubel.
Kulatý stůl se konal díky laskavé podpoře Všeobecné zdravotní pojišťovny a Asociace inovativního farmaceutického průmyslu.
Michaela Koubová
Foto: Radek Čepelák

