Generické léky jsou dnes součástí péče, která takříkajíc zachraňuje lékový budget veřejného zdravotního pojištění před nárůstem, jenž v posledních letech zaznamenáváme u centrové péče. Prostřednictvím rychlého vstupu i dalších opatření se daří snižovat cenové hladiny celých lékových skupin a díky tomu zpřístupňovat léčbu většímu množství pacientů. Množství generik na trhu navíc pomáhá bojovat i proti dalšímu, stále akutnějšímu problému – totiž nedostatku některých léků. Právě od spolupráce s výrobci generik si ministerstvo zdravotnictví slibuje možnost najít nová řešení, jak se s problémem výpadků vypořádat u co největšího množství přípravků. Na druhou stranu ale výrobci doufají, že získají pomocnou ruku v rámci Evropy v souvislosti s nyní projednávaným osvobozením od SPC pro výrobu léčiv v unii. Možnost prodloužení patentové ochrany o pět let totiž v současnosti nutí farmaceutické společnosti, které chtějí konkurovat i na jiných než evropských trzích, aby přesouvaly výrobu mimo EU. O problematice diskutovali odborníci na kulatém stole Zdravotnického deníku s názvem Jak posílit roli generik a biosimilars ve zvyšování dostupnosti zdravotní péče a nákladové efektivity, který se konal minulý pátek v Praze.
„Česká republika dnes patří díky mechanizmům v zákoně o veřejném zdravotním pojištění, tedy rychlému, zkrácenému vstupu generik, mezi země velmi rychlé. Naše křivka se z mých zkušeností podobá spíše křivce Německa či Británie než rezistentnějším zemím jižního křídla,“ konstatuje ředitel Value Outcomes s.r.o. Tomáš Doležal.
Česko má zakotvený zrychlený vstup během třicetidenní lhůty od roku 2011 a systém dosud funguje velmi hladce. „Nenastávají žádné problémy, takže to nemáme v plánu nikterak rušit. Naopak budeme hledat další cesty, jak pomoci v jiných oblastech,“ uvádí náměstek ministra zdravotnictví Filip Vrubel. To potvrzuje i Tomáš Doležal. „Ve vstupu generik na trh nemáme moc co napravovat. Máme institut podobného přípravku, máme zkrácené řízení, SÚKL nemá problémy odbavovat, takže generika vstupují velmi rychle a velmi rychle mají i možnost stlačit cenu originálu. To není v Evropě zcela standardní – tam se ceny generik a originálů často po nějakou dobu výrazně liší. Třetí bod je otázka využití a rozšířenosti generik v reálném životě, kde existují nástroje zdravotních pojišťoven, jako jsou pozitivní listy. Tam se můžeme bavit, zda jsou dnes pojišťovny schopny a ochotny vymoci si preskripci pozitivního listu, a jestli nejsou přebíjeny pozitivními listy poskytovatelů nebo lékárnických řetězců. Myslím si, že často sílu nemají,“ poukazuje Doležal.

Je ovšem otázka, co vlastně samy pojišťovny od svých pozitivních listů očekávají. Svaz zdravotních pojišťoven si od nich slibuje hlavně cenovou soutěž na trhu. „Rozhodnutí, co použít, má udělat lékař, k tomu pojišťovna nemůže moc nutit. Může ale motivovat a vyvolávat cenové soutěže – jakmile jedna firma sníží cenu, aby se dostala na pozitivní list, další se tomu tiše přizpůsobí,“ říká Ivana Cimalová, ředitelka odboru zdravotnického Zdravotní pojišťovny Ministerstva vnitra.
Alena Miková, ředitelka Odboru léčiv a zdravotnických prostředků Všeobecné zdravotní pojišťovny, k tomu dodává, že 80 procent preskriptorů má v rámci svých softwarů doporučení z pozitivních listů VZP a zpětně také dostávají echo o tom, nakolik potenciál využili.
Mohlo by vás zaujímať
Informovanost ohledně generik chce podporovat i ministerstvo zdravotnictví v rámci eReceptu, kde má vedle generické preskripce lékař nově možnost zjistit, jaký lék byl ve finále v lékárně vydán. „Zabýváme se také tím, jak více podpořit, aby s poklesem nákladů docházelo k šíření preskripce, částečně směrem k praktickým lékařům,“ poukazuje Filip Vrubel. V tuto chvíli je ovšem podle něj systém nastaven chybně, protože rozšíření preskripce má navrhovat držitel registrace nebo zdravotní pojišťovna, což se ne vždy děje. Tomáš Doležal zase upozorňuje, že k rozšíření preskripce je třeba kývnutí ambulantních specialistů, kteří ale nezřídka bývají proti zkrátka proto, aby nepřišli o pacienty.
„Vidím to jako námět na legislativní změnu a u preskripčních omezení je třeba reagovat z gruntu. Nemyslím jen rozšíření stávajících preskripčních omezení. Současnému systému vyčítám, že SÚKL, potažmo odvolací orgán, neumí ve správním řízení zohlednit, že je tu vyšší princip. Na jednu stranu ministerstvo říká, že chce posílit kompetence praktických lékařů, ale zároveň ministerstvo jako správní odvolací orgán podporuje SÚKL v tom, že žádné rozšiřování mezi praktickými lékaři není,“ vysvětluje Vrubel.
Peníze putují na větší dostupnost léčby i centrovou péči
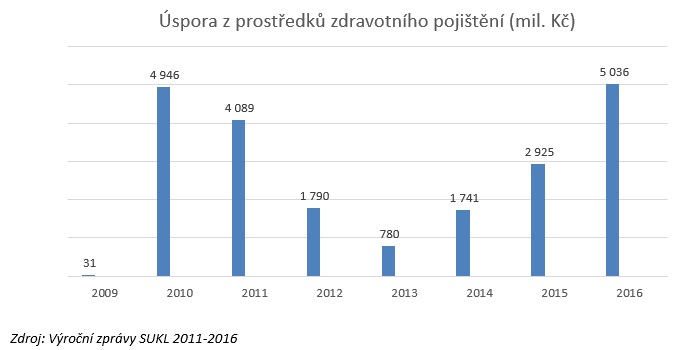
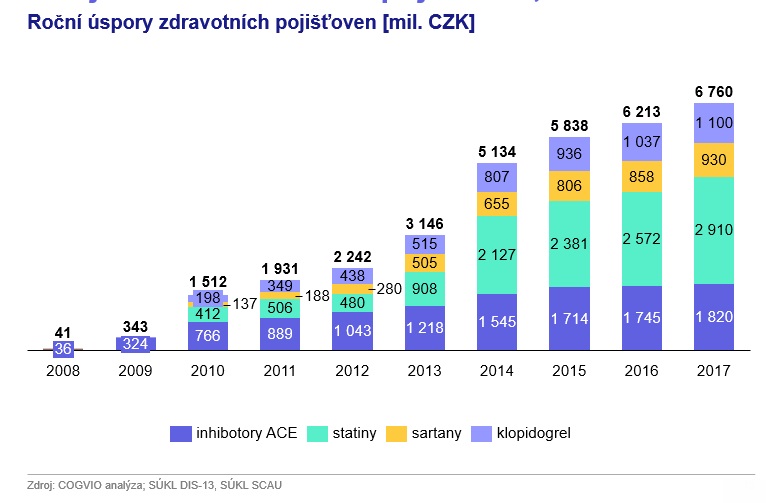
Kolik prostředků vlastně dnes generika ušetří? Pokud by podle čísel SÚKL od roku 2008 do 2018 neprobíhaly u generických přípravků hloubkové revize, kterých byly stovky, vyšplhaly by se náklady na léčivé přípravky o skoro 16 miliard korun výše. A hloubkové revize nejsou jediným nástrojem, který pomáhá ceny snižovat. Podle studie pro společnost Teva týkající se kumulativních úspor v oblasti kardiologie se v posledních deseti letech díky generikům ušetřilo dohromady až 33 miliard (nejvíce na statinech, kde šlo o 12 miliard, dále na ACE inhibitorech – 11 miliard, kolpidogrelu – přes pět miliard, a sartanech – čtyři miliardy). Potenciál úspor dosažených díky generikům jen u VZP pak ilustruje doktorka Miková na případu ezetimibu na vysoký cholesterol, za který dala loni pojišťovna 214 milionů, po uzavření dohody o nejvyšší ceně výrobce (DNCV) se ale povedlo srazit cenu o 83 procent. Očekávaná úspora tak činí 180 milionů, zároveň by ovšem v duchu výše popsané snahy mělo dojít k úpravě indikačního a preskripčního omezení tak, že se lék dostane k většímu počtu pacientů.
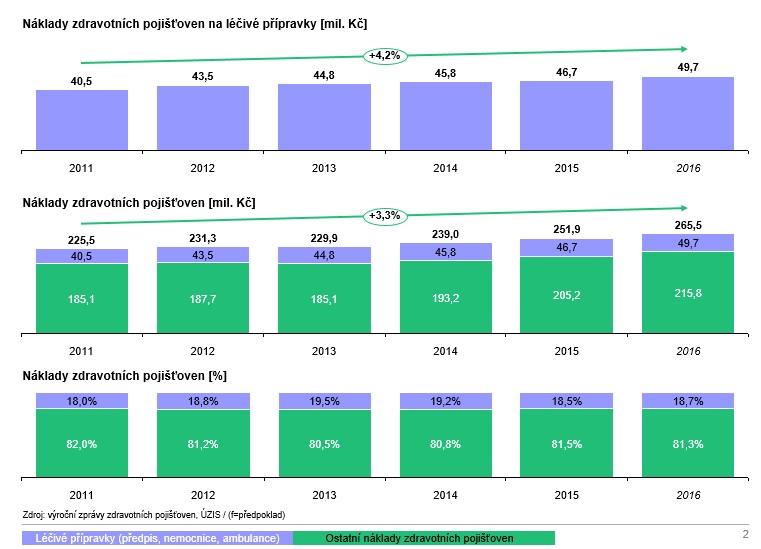
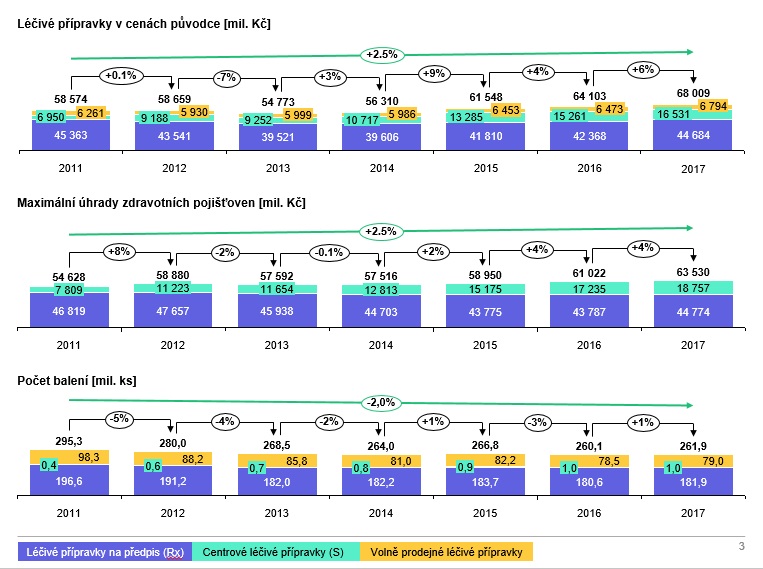
Podíl generik se přitom daří zvyšovat – od roku 2011 vzrostl z 49,5 na 57,9 procenta v loňském roce. Náklady na léky celkově ovšem mezi lety 2011 a 2016 mírně vzrostly, i když jen o necelých pět procent. Důvodem jsou rychle stoupající centrová léčiva, jejichž často i dvouciferný meziroční růst vyrovnávají receptové léky, které naopak prostředky šetří.
Na druhou stranu je pravda, že cenová regulace léků u nás může některé výrobce a distributory odrazovat. Zájem registrovat se na českém trhu je poměrně velký, s jednáním o úhradě je to ale horší. To, že se dokonce výrobci rozhodnou odejít z našeho trhu kvůli nízké ceně, pak stojí za třemi procenty výpadků léků.
Oblast reexportů zřejmě čeká další úprava, ta dosavadní nefunguje
Vedle úspor mají ovšem generika ještě další nezanedbatelný přínos. Nejen v Česku, ale celosvětově totiž v posledních letech narůstá problém s nedostupností léčiv. „To se v oblastech, kde je dostatečná generifikace a konkurence, nevyskytuje. Dostatek generik tak je zárukou dostupnosti léků pro pacienty,“ poukazuje výkonný ředitel České asociace farmaceutických firem Martin Mátl. V tomto směru by mělo zájem s generickým průmyslem spolupracovat ministerstvo zdravotnictví, které se chce zabývat opatřeními zajišťujícími dostupnost léků. Výpadky totiž nepostihují jen léky nové, nýbrž i ty dlouho zavedené.
Jaká řešení se nabízí? „Máme nevýhodu, že jsme malý a ne úplně významný trh i pro generický průmysl. Není úplně možné představit si, že by si Česká republika zajistila výrobu léků pro svůj trh sama. Na druhou stranu pokud tu bude vůle, umím si představit, že jestliže jsou léky vyráběny alespoň někde jinde v EU a z nějakého důvodu se na český trh nedostávají, mohly by být pobídky pro dodávky na český trh. Před několika lety jsme diskutovali s odbornou veřejností myšlenku, že u některých esenciálních léků, které se nedostávají na český trh a je zjevné, že se bude problematika nedostupnosti opakovat, by bylo v zájmu státu domluvit se s některým distributorem v rámci veřejného tendru a nakoupit léky ve prospěch státu v zahraničí. Stát by držel nepodkročitelnou zásobu, kterou by pak pouštěl do distribučního řetězce, aby byly naplněny požadavky českých pacientů,“ načrtává Vrubel.
Dalším aspektem pak jsou reexporty způsobené nízkou cenou léčiv na českém trhu. Ty přitom provádí zhruba sedmdesát distributorů (17 procent jejich celkového počtu v ČR) a zahrnují 1,5 až pět procent z celkového objemu distribuovaných léků. Náměstek Vrubel přitom uznává, že nástroje, které se loni dostaly do legislativy s tím, že mají reexportům zabránit, nejsou zcela účinné. „Hledáme způsoby, jak to nahradit. Už jsme na tom se SÚKL několikrát seděli a máme určitou myšlenku. V rámci letních měsíců bychom chtěli s odbornou veřejností prodiskutovat, jak by to mohlo v České republice vypadat,“ říká náměstek Vrubel.
Jeho slova potvrzuje pověřená šéfka SÚKL Irena Storová. „Paragraf 77 (práva a povinnosti distributora, pozn. red.) je nevymahatelný a nerealizovatelný. Začali jsme se proto bavit o novelizaci a asi se z velké části inspirujeme slovenským modelem. Slovensko je stát, který je nastaven podobně jako my a už to tam mají nějakou dobu aktivní, díky čemuž máme i informace o tom, kde jsou slabá místa, která bychom byli schopni preventovat,“ přibližuje Storová.
EU přemýšlí o výjimce pro výrobu v době platnosti SPC
Obecně je však nejčastější příčinou nedostupnosti léků nejen u nás problém ve výrobě. „Dnes se na evropské úrovni vytváří skupina expertů ze všech států EU, která nedostatky léků řeší. Vůbec to tedy není náš národní problém. V nejčernějším scénáři se může stát, že když výrobce soustředí výrobu do třetích zemí nebo jinam a je jediný dodavatel aktivní substance, tak ve chvíli, kdy vypadne, nás to postihne všechny,“ dodává Irena Storová.

Urychlit vstup generik na evropské úrovni spolu s pomocnou rukou generickému průmyslu tak, aby nebyl vytlačován za hranice EU, by přitom mohla změna související s dodatkovým ochranným osvědčením (SPC). Toto evropské opatření prodlužuje ochranu patentovaných léčiv až o pět let tak, aby se podporovaly investice do výzkumu a vývoje. „Má to ale jeden nezamýšlený efekt. Pokud chce výrobce, který je usazený v EU, konkurovat jiným výrobcům třeba na americkém trhu, dostává se do nevýhody a je nucen přesouvat svou výrobu mimo EU,“ vysvětluje Martin Mátl.
Evropská komise přitom zveřejnila studii o dopadu osvobození od SPC, která ukazuje, že by krok znamenal pro EU zvýšení čistých prodejů ve farmaceutickém průmyslu do roku 2025 o 9,5 miliardy eur, vytvoření 25 tisíc nových pracovních míst a úspory na farmaceutických výdajích v EU ve výši 3,1 miliardy eur. Evropský parlament tak již několikrát vyzval Evropskou komisi, aby osvobození od SPC pro výrobu léčiv zavedla.
„Je to téma, které teď bude v legislativním procesu EU nějakou dobu velmi významné. Bude se jednat o výjimce, která by umožnila vyrábět v EU v době platnosti SPC, a bylo by dobré, kdyby Česká republika ke hlasu také nějakým způsobem přispěla,“ dodává Mátl. „Česká republika může podpořit snahu generického průmyslu, jednáme o tom s panem ministrem,“ reaguje Filip Vrubel.
Podle Mátla by měl nový legislativní návrh umožnit firmám připravit se na okamžité uvedení na trh od prvního dne po vypršení platnosti patentové ochrany v Evropě, protože až v 80 procentech případů končí doba platnosti ochrany účinných látek v EU později než v jinde ve světě. V případě léků vyžadujících velké investice do vývoje a výroby, jako jsou například biosimilars, je přitom možnost přípravy na okamžité uvedení na trh od prvního dne v rámci EU klíčovým kritériem pro umístění souvisejících provozů do Evropy.
Problematice biosimilars se budeme věnovat v nadcházejících vydáních ZD.
Kulatý stůl se konal díky laskavé podpoře České asociace farmaceutických firem a Zdravotní pojišťovny Ministerstva vnitra ČR.
Michaela Koubová, foto: Martin Kovář

